磷酸钠溶液中的三大守恒
1、物料守恒:Na⁺=3H₃PO₄+3H₂PO₄⁻+3HPO₄²⁻+3PO₄³⁻
磷酸钠溶液中某一组分的原始浓度应该等于它在溶液中各种存在形式的浓度之和。也就是元素守恒(原子守恒),变化前后某种元素的原子个数守恒不变。
2、电荷守恒:Na⁺+H⁺=OH⁻+3PO₄³⁻+2HPO₄²⁻+H₂PO₄⁻
溶液永远是电中性的,所以阳离子带的正电荷总量=阴离子带的负电荷总量。
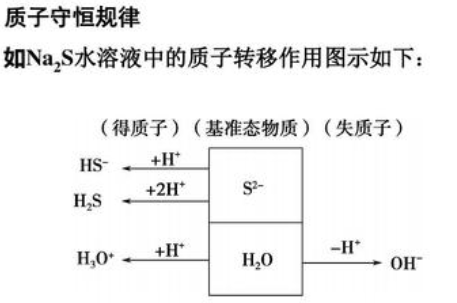
3、质子守恒,H⁺+HPO₄²⁻+2H₂PO₄⁻+3H₃PO₄=OH⁻
酸失去的质子和碱得到的质子数目相同。
扩展资料
1、物料守恒的特点:
“任一化学反应前后原子种类和数量分别保持不变”,可以微观地应用到具体反应方程式,就是左边带电代数和等于右边。其中的也可以理解为原子核,因为外围电子数可能有变,这时候可以结合电荷守恒来判断问题。
2、电荷守恒的注意事项
(1)化合物中元素正负化合价代数和为零
(2)溶液呈电中性:所有阳离子所带正电荷总数等于阴离子所带负电荷总数
(3)除六大强酸,四大强碱外都水解,多元弱酸部分水解。产物中有部分水解时产物
(4)这个离子所带的电荷数是多少,离子前写几。
参考资料来源:百度百科-物料守恒
参考资料来源:百度百科-电荷守恒
参考资料来源:百度百科-质子守恒
声明:本网站引用、摘录或转载内容仅供网站访问者交流或参考,不代表本站立场,如存在版权或非法内容,请联系站长删除,联系邮箱:site.kefu@qq.com。