o2+,o2,o2-,o22-的稳定性是什么
分子轨道式如图所示:
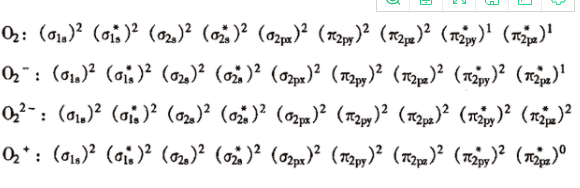
键级分别为2、1.5、1、2.5(键级=(成键电子数-反键电子数)/2)。
所以稳定性:O2 + > O2 > O2 - > O2 2-。
类型:
在价键理论当中共价键可以分为σ和π键。在分子轨道当中我们如何区别它们呢?在氢分子离子形成过程当中我们看到了由两个1s轨道形成了一个成键的σ1s轨道(形状像橄榄)和另一个反键σ1s*(形状像两个鸡蛋)。凡是分子轨道对称轴形成圆柱形对称的叫做“σ轨道”。
在成键δ轨道上的电子称为“成键σ电子”,它们使得分子稳定化;在反键δ*轨道上的电子称为“反键σ电子”,它们使得分子有解离的倾向。由成键σ电子构成的共价键称为δ键。
同样,我们可以用参加组合的原子轨道图形,按照一定的重叠方式定性的绘出其他的分子轨道。比如沿着x轴靠近则两个px轨道将“头碰头”的组成两个σ型分子轨道,如果是py和py,pz和pz就是“肩并肩”的组合称为另一种形状的分子轨道,称为π轨道。
声明:本网站引用、摘录或转载内容仅供网站访问者交流或参考,不代表本站立场,如存在版权或非法内容,请联系站长删除,联系邮箱:site.kefu@qq.com。
阅读量:26
阅读量:74
阅读量:101
阅读量:27
阅读量:47