反应进度怎么算
1、第一步 化学反应中反应物(消耗)的量或生成物(增加)的量可根据反应方程式的计量系数与生成物量的变化进行相互换算。
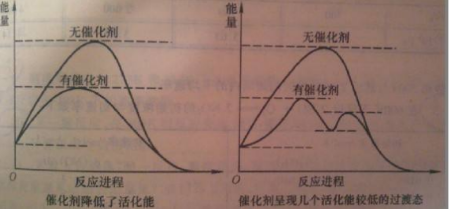
2、下一步 如式子反应中:N2+ 3 H2→ 2 NH3 系统中,如N2消耗1mol,H2即消耗3mol,生成物NH3则增加2mol。因此,用不同的反应物或生成物"物质的量"的变化来表示化学反应进行程度的数值各异,在使用上带来不便。
3、下一步 人们将反应系统中任何一种反应物或生成物在反应过程中物质的量的变化△nB与该物质的计量系数vB的商定义为该反应的反应进度,记为:ξ= △nB/vB
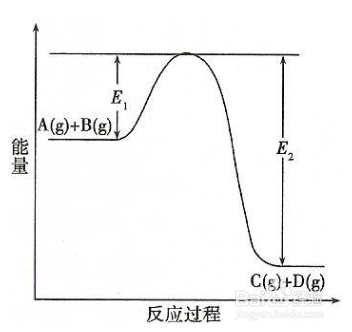
4、最后 化学反应的反应速率是相关受质浓度随时间改变的的测量。反应速率的分析有许多重要应用,像是化学工程学或化学平衡研究。反应速率与参与反应的物质浓度有关。物质浓度则可透过质量作用定律定量。
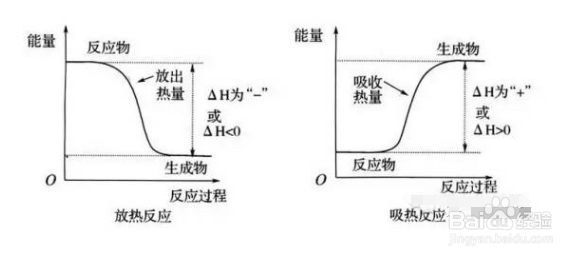
1、化学反应中反应物(消耗)的量或生成物(增加)的量可根据反应方程式的计量系数与生成物量的变化进行相互换算。
2、N2+ 3 H2→ 2 NH3 系统中,如N2消耗1mol,H2即消耗3mol,生成物NH3则增加2mol。
3、人们将反应系统中任何一种反应物或生成物在反应过程中物质的量的变化△nB与该物质的计量系数vB的商定义为该反应的反应进度,记为:ξ= △nB/vB
声明:本网站引用、摘录或转载内容仅供网站访问者交流或参考,不代表本站立场,如存在版权或非法内容,请联系站长删除,联系邮箱:site.kefu@qq.com。